बफर विलयन
उभय-प्रतिरोधी विलयन या बफर विलयन (buffer solution) किसी दुर्बल अम्ल तथा उसके संयुग्मी क्षारक अथवा किसी दुर्बल क्षारक एवं उसके संयुग्मी अम्ल का जलीय विलयन होता है। बफर बिलयन का मुख्य गुण यह है कि इसमें किसी प्रबल अम्ल या प्रबल क्षारक की थोड़ी मात्रा या मध्यम मात्रा मिलाने पर भी इसका पीएच बहुत कम बदलता है।
जीवविज्ञान में प्रयुक्त सामान्य बफर यौगिक
संपादित करें| सामान्य नाम | संरचना | pKa 25 °C पर |
ताप का प्रभाव dpH/dT in (1/K)[1] |
Mol. Weight |
|---|---|---|---|---|
| TAPS | 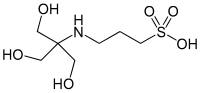 |
8.43 | −0.018 | 243.3 |
| Bicine |  |
8.35 | −0.018 | 163.2 |
| Tris |  |
8.06 | −0.028 | 121.14 |
| Tricine | 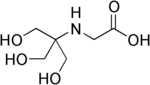 |
8.05 | −0.021 | 179.2 |
| TAPSO |  |
7.635 | 259.3 | |
| HEPES |  |
7.48 | −0.014 | 238.3 |
| TES | 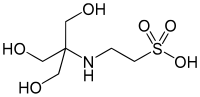 |
7.40 | −0.020 | 229.20 |
| MOPS |  |
7.20 | −0.015 | 209.3 |
| PIPES | 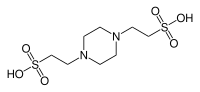 |
6.76 | −0.008 | 302.4 |
| Cacodylate | 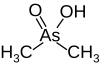 |
6.27 | 138.0 | |
| MES | 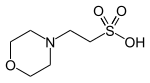 |
6.15 | −0.011 | 195.2 |
सन्दर्भ
संपादित करें- ↑ "Buffer Reference Center". Sigma-Aldrich. मूल से 17 अप्रैल 2009 को पुरालेखित. अभिगमन तिथि 2009-04-17.