हाइड्राज़िन
हाइड्रेज़ीन (Hydrazine / H2N-NH2) अकार्बनिक यौगिक है जिसका अणुसूत्र N2H4 है। यह रंगहीन, ज्वलनशील द्रव है जिसमें अमोनिया जैसी गंध आती है। इसे डायाजेन (diazane) भी कहते हैं। यह अत्यन्त विषैली तथा भयानक अस्थिर है इसलिये इसे इसे विलयन में ही रखा जाता है। हाइड्रेजीन मुख्यतः पॉलीमर फोम के निर्माण में 'फोमिंग एजेंट' के रूप में प्रयुक्त होती है। इसके अलावा यह बहुलीकारक उत्प्रेरक के उपयोग के पूर्व उपयोग की जाती है। औषधि निर्माण में भी इसका उपयोग है। यह रॉकेट के ईंधन में प्रयुक्त होती है। यह नाभिकीय और गैर-नाभिकीय विद्युत शक्ति संयंत्रों के वाष्प चक्र (steam cycles) में घुलित आक्सीजन की सांद्रता को कम करने के लिये प्रयुक्त होती है ताकि संक्षारण (corrosion) को कम किया जा सके।
| हाइड्राज़िन | |
|---|---|
 |
 |
 |
 |
| प्रणालीगत नाम | हाइड्राज़िन[1] |
| अन्य नाम | डीयामाइनDiamine[उद्धरण चाहिए] Diazane[1] |
| पहचान आइडेन्टिफायर्स | |
| सी.ए.एस संख्या | [302-01-2][CAS] |
| पबकैम | |
| EC संख्या | |
| UN संख्या | 2029 |
| केईजीजी | C05361 |
| MeSH | Hydrazine |
| रासा.ई.बी.आई | 15571 |
| RTECS number | MU7175000 |
| SMILES | |
| InChI | |
| 878137 | |
| जी-मेलिन संदर्भ | 190 |
| कैमस्पाइडर आई.डी | |
| 3DMet | {{{3DMet}}} |
| गुण | |
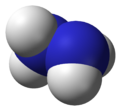
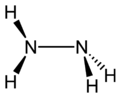
| आण्विक सूत्र | N2H4 |
| मोलर द्रव्यमान | 32.0452 g mol-1 |
| दिखावट | रंगहीन द्रव्य |
| घनत्व | 1.021 g cm-3 |
| गलनांक |
2 °C, 275 K, 35 °F |
| क्वथनांक |
114 °C, 387 K, 237 °F |
| log P | 0.67 |
| वाष्प दबाव | 1 kP (at 30.7 °C) |
| अम्लता (pKa) | 8.10[2] |
| Basicity (pKb) | 5.90 |
| रिफ्रेक्टिव इंडेक्स (nD) | 1.46044 (at 22 °C) |
| श्यानता | 0.876 cP |
| ढांचा | |
| आण्विक आकार | N पर त्रिकोणाकार पिरामिड |
| Dipole moment | 1.85 D[3] |
| मानक मोलीय एन्ट्रॉपी S |
121.52. J K-1 mol-1 |
| खतरा | |
| एम.एस.डी.एस | ICSC 0281 |
| EU वर्गीकरण | साँचा:Hazchem T साँचा:Hazchem N |
| EU सूचकांक | 007-008-00-3 |
| NFPA 704 | |
| R-फ्रेसेज़ | साँचा:R45, साँचा:R10, साँचा:R23/24/25, R34, साँचा:R43, साँचा:R50/53 |
| S-फ्रेसेज़ | साँचा:S53, S45, साँचा:S60, S61 |
| स्फुरांक (फ्लैश पॉइन्ट) | 52 °C |
| स्वयंप्रजवलन तापमान |
24–270 °C |
| Explosive limits | 1.8–99.99% |
| एलडी५० | 59–60 mg/kg (oral in rats, mice)[4] |
| Related compounds | |
| संबंधित रसायन/मिश्रण | अमोनिया |
| जहां दिया है वहां के अलावा, ये आंकड़े पदार्थ की मानक स्थिति (२५ °से, १०० कि.पा के अनुसार हैं। ज्ञानसन्दूक के संदर्भ | |
परिचय
संपादित करेंहाइडेजीन का क्वथनांक 114.5° सें., गलनांक 2.0° सें. है। यह कर्टियस द्वारा 1887 ई. में पहले पहल तैयार हुआ था। आजकल राशिग विधि (Rashig Method) से यह तैयार होता है। इस विधि में यह जलीय अमोनिया या यूरिया को जिलेटीन या ग्लू की उपस्थिति में हाइपोक्रोइट के आधिक्य में ऑक्सीकरण से तैयार किया जाता है। यह अभिक्रिया 160° - 180° से. ताप पर दबाव में संपन्न होती है और 2% की मात्रा में हाइड्रेज़ीन बनता है जिसके आंशिक आवन द्वारा सांद्रण से 60-65% हाइड्रेज़ीन प्राप्त होता है। इससे बेरियम आक्साइड, दाहक सोडा या पोटाश द्वारा निर्जलीकरण से अजल हाइड्रेज़ीन प्राप्त हो सकता है। अजल हाइड्रेज़ीन जल, मेथिल और एथिल ऐल्कोहॉल में सब अनुपात में मिश्र होता है। जलीय विलयन अमोनिया की अपेक्षा दुर्बल क्षारीय होता है, यह दो श्रेणी का लवण, क्लोराइड आदि, बनाता है। जलीय विलयन में हाइड्रेज़ीन प्रबल अपचायक होता है। ताँबे, चाँदी और सोने के लवणों से धातुओं को यह अवक्षिप्त कर देता है। द्वितीय विश्वयुद्ध में ईधंन के रूप में राकेट और जेट नोदक में यह प्रयुक्त हुआ था। इसको बड़ी सावधानी से संग्रह करने की आवश्यकता होती है क्योंकि यह सरलता से आर्द्रता, कार्बन डाइआक्साइड और ऑक्सीजन से अभिक्रिया देता है। इसके विलयन तथा वाष्प दोनों विषैले होते हैं। हाइड्रेज़ीन के वाष्प और वायु के मिश्रण जलते हैं।
हाइड्रेज़ीन के हाइड्रोजन कार्बनिक मूलकों द्वारा सरलता से विस्थापित होकर अनेक कार्बनिक संजात (derivatives) बनते हैं। एक ऐसा ही संजात फेनिल हाइड्रेज़ीन है जिसका आविष्कार एमिल फिशर ने 1877 ई. में किया था। इसकी सहायता से उन्होंने कार्बोहाइड्रेटों के अध्ययन में पर्याप्त प्रगति की थी। हाइड्रेज़ीन का एक दूसरा संजात अम्ल हाइड्रेज़ाइड (RCO2 N2 H4) है जो अम्ल क्लोराइड या एस्टर पर हाइड्रेज़ीन की अभिक्रिया से बनता है। ऐसे दो संजात सेमी कार्बेज़ाइड, CO (NH2) N2 H3 और कार्बोहाइड्रेज़ाइड CO(N2 H3)2 हैं जिनका उपयोग वैश्लेषिक रसायन में विशेष रूप से होता है।
सन्दर्भ
संपादित करें- ↑ अ आ "hydrazine - PubChem Public Chemical Database". The PubChem Project. USA: National Center for Biotechnology Information. मूल से 8 मार्च 2012 को पुरालेखित. अभिगमन तिथि 31 मार्च 2012.
- ↑ Hall, H.K., J. Am. Chem. Soc., 1957, 79, 5441.
- ↑ साँचा:Greenwood&Earnshaw2nd
- ↑ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. पृ॰ 361. आई॰ऍस॰बी॰ऍन॰ 1903996651.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
