बेरियम
बेरियम (Barium) कैल्सियम समूह का तत्व है। खनिज बेराइट इसका पहला खनिज था, जिसकी ओर सन् 1602 में बोलोन के एक चर्मकार बी. केसिओरलस का ध्यान गया। उसने देखा कि यह पदार्थ दहनशील पदार्थ के साथ जलने पर स्फुरदीप्त होता है। इसी कारण इसका बोलोनी फॉस्फोरस भी कहा जाता है। सन् 1774 में के.डब्ल्यू शीले ने पाइरोल्यूसाइट खनिज की जाँच करते समय एक नई मृदा मालूम की, जिसे टी.ओ. वर्गमैन (Bergman) ने भारी मृदा (Terra Ponderosa) कहा। सन् 1779 में लूई बर्नार्ड गितों द मोरवां (Louis Bernard Guyton de Morvean) न इसे बेरोट (Barote) नाम दिया, जिस लवाज़िए (Lavoisier) ने बदलकर बेराइटा कर दिया। आज भी इस मृदा के लिए यह नाम प्रचलित है। ग्रीक शब्द बेरस (Barus) से, जिसका अर्थ भारी है, यह बना है। बाद में मालूम हुआ कि यह एक नई धातु का ऑक्साइड है। इसी के नाम पर इस धातु को बेरियम कहा जाने लगा।
| बेरियम / Barium रासायनिक तत्व | |
 | |
| रासायनिक चिन्ह: | Ba |
| परमाणु संख्या: | 56 |
| रासायनिक शृंखला: | क्षारीय पार्थिव धातु |
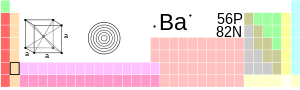 आवर्त सारणी में स्थिति
| |
 | |
| अन्य भाषाओं में नाम: | Barium (अंग्रेज़ी), Барий (रूसी), バリウム (जापानी) |
परिचय
संपादित करेंबेरियम धातु प्रकृति में शुद्ध रूप में नहीं मिलती। इसके प्रसिद्ध खनिज कार्बोनेट लवण, अर्थात् विदराइट (witherite) और सल्फेट लवण, अर्थात् बाराइटीज के रूप में मिलते हैं। थोड़ी मात्रा में यह धातु बेराइटो कैल्साइट, बेराइटो सेलिसटाइन और अन्य सिलिकेट लवणों में भी मिलती है। सिलोमेलेन (Psilomelane), अर्थात् बेरियम मैगनेटाइट, भी इसका एक खनिज है। भारत में बराइटीज खनिज बहुत पाया जाता है। मद्रास के अर्नूल और अलवर क्षेत्र इसके लिए प्रसिद्ध है।
बेरियम का ऑक्सीजन के प्रति इतना आकर्षण है कि शुद्ध धातु को प्राप्त करना बड़ा कठिन हो गया है। सन् 1808 में डेवी ने बेरियम संरस तैयार किया। इस संरस को सुखाकर और फिर इसके पारे का आसवन कर बेरियम धातु तैयार की। इस विधि में दो कठिनाइयाँ आती हैं। एक तो सरंस में पानी पूर्णत: सुखा लेना आवश्यक है, दूसरे ऊँचे ताप पर भी बेरियम से पारा पूर्णत: अलग नहीं होता। सन् 1901 में गुंट्ज (Gunts) ने 1,200 डिग्री सें. पर बेरियम ऑक्साइड का ऐल्यूमिनियम चूर्ण द्वारा अपचयन करके बेरियम प्राप्त किया। इसी ताप पर सी. मैटिग्नॉन (Matignon) ने निर्वात में फेरोसिलिकन (95 प्रतिशत सिलिकन) के साथ अपचयित कर 98.5 प्रतिशत शुद्ध बेरियम का आसवन किया। आज भी ये ही विधियाँ प्रयोग में आती हैं।
बेरियम सफेद नर्म धातु है। इसका परमाणुभार 137.37, परमाणु क्रमांक 56, घनत्व 3.78, गलनांक 850 डिग्री सें. और क्वथनांक 1,537 डिग्री सें. है। इसकी सयोजकताएँ दो हैं। एक ही श्रेणी के यौगिक बनाता है। पानी में विलेय है और हाइड्रॉक्साइड बनाता है। क्षारों और अम्लो में विलेय है। बेंज़ीन और हाइड्रोकार्बनों में अविलेय है। इसके चूर्ण को हवा में छोड़ दें तो यह जल उठता है। यह सीसे के समान आघातवर्धनीय है। ऐल्कोहॉल के साथ यह बेरियम ऐंथॉक्साइड बनाता है। केल्सियम से इस बात में भिन्न है।
प्राकृत कार्बोनेट पर नाइट्रिक अम्ल की अभिक्रिया से नाइट्रेट बनता है। नाइट्रेट अधिक ताप पर बेराइटा, अर्थात् बेरियम मॉनोआक्साइड (BaO), में बदल जाता है। इसको हवा में धीरे से गरम करने पर यह बेरियम डाइऑक्साइड में (Ba O2) में बदल जाता है। डाइऑक्साइड को अधिक ताप पर गरम करने से आक्सीजन और बेरियम मोनो-ऑक्साइड मिलता है। इस अभिक्रिया का प्रयोग ऑक्सीजन बनाने की ब्रिन विधि में किया जाता है। इसका एक तीसरा ऑक्साइड बेरियम सबऑक्साइड, (Ba2O), भी मिलता है।
बेराइटा पानी में विलेय होकर हाइड्रॉक्साइड देता है। इसके विलयन की उपयोगिता अनुमापन में है, क्योंकि यह कार्बन डाइऑक्साइड से सदा मुक्त रहता है। जो कुछ कार्बन डाइऑक्साइड गैस अवशोषित हुई, वह अविलेय बेरियम कार्बोनेट बनकर पृथक् हो जाती है। यह विशेषता अन्य क्षारीय विलयनों, जैसे दाहक सोडा और ऐमोनिया, में नहीं है। इसका उपयोग चीनी को साफ करने के लिए भी होता है।
किसी भी सल्फेट विलयन में किसी बेरियम लवण का विलयन डालने से बेरियम सल्फेट का सफेद अवक्षेप मिलता है। इसी गुणधर्म के कारण बेरियम के विलेय लवण, विशेष तौर पर बेरियम क्लोराइड, का सलफ्यूरिक अम्ल और सल्फेट लवणों की जाँच के लिए प्रयोग होता है। वर्णक उद्योग में बेरियम सल्फेट का अधिक उपयोग होता है। ब्लांक फिक्से (Blanc Fixe) और लिथोपोन (Lithopone) इसके प्रसिद्ध वर्णक हैं। बेरियम कार्बोनेट और हाइड्रोक्लोरिक अम्ल की अभिक्रिया से बेरियम क्लोराइड बनता है। बेरियम के विलेय लवणों में यह सबसे अधिक प्रसिद्ध है। इसके विलेय लवण विषैले होते हैं।
सभी बेरियम लवण बुंसन ज्वाला को हरा रंग देते हैं। इसके विलये लवण कैल्सियम सल्फेट के साथ सफेद अवक्षेप देते हैं और पोटैशियम क्रोमेट के विलयन के साथ बेरियम क्रोमेट का पीला अवक्षेप देते हैं।