टाइटेनियम
टाइटेनियम एक मजबूत धातु है। इस तत्व का सबसे पहले सन् 1791 में ग्रेटर ने पता लगाया तथा सन् 1795 में क्लापराथ ने इसका नाम टाइटेनियम रखा। इसके मुख्य खनिज इलमिनाइट तथा रुटाइल हैं। दूसरे खनिज स्थुडोब्रुकाइट, (Fe4 (TiO4) 3), एरीजोनाइट, (Fe2 (TiO3)3), गाइकीलाइट (MgTiO3) तथा पायरोफेनाइट, (MnTiO3) इत्यादि हैं
| टाइटेनियम / Titanium रासायनिक तत्व | |
 | |
| रासायनिक चिन्ह: | Ti |
| परमाणु संख्या: | 22 |
| रासायनिक शृंखला: | संक्रमण धातु |
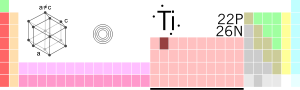 आवर्त सारणी में स्थिति
| |
 | |
| अन्य भाषाओं में नाम: | Titanium (अंग्रेज़ी), Титан (रूसी), チタン (जापानी) |
धातु के क्लोराइड के वाष्प को द्रवित सोडियम के ऊपर से पारित करने पर, अथवा पोटासियम के साथ अवकरण से, अथवा धातु के हेलोजन लवण या ऑक्साइड के कैल्सियम, मैग्नीशियम या ऐल्यूमिनियम द्वारा अवकरण से यह धातु प्राप्त होती है। बुसे (सन् 1853) ने पोटासियम टाइटेनेट, सोडियम सल्फेट और सल्फयूरिक अम्ल के विद्युद्विच्छेदन द्वारा सफेद टाइटेनियम प्राप्त किया था। यह दुनिया की सबसे मजबूत धातुअओं में एक है।[1]
गुणधर्म
संपादित करेंयह लोहे जैसी धातु है। इसका आपेक्षिक घनत्व 3.49 से 3.59 तक तथा द्रवणांक लगभग 2,000 सें0 है। यह हवा में स्थायी है, परंतु 1,200 डिग्री सें0 ताप तक गरम करने पर टाइटेनियम ऑक्साइड, (TiO2), बनता है हैलोजन सरलता से इस धातु को आक्रांत करते हैं। फ्लोरीन सबसे आसानी से तथा आयोडीन देर में और ऊँचे ताप पर आक्रांत करता है। यह नाइट्रोजन, फॉस्फोरस, बोरॉन तथा सल्फर से ऊँचे ताप पर क्रिया करके नाइट्राइड, फॉस्फाइड, बोराइड तथा सल्फाइड बनाती है। हाइड्रोक्लोरिक अम्ल, सल्फ्यूरिक अम्ल तथा नाइट्रिक अम्ल इसको सरलता से आक्रांत करते हैं। ऑक्सीकारक पदार्थ जैसे पोटासियम क्लोरेट, पोटासियम परमैंगेनेट इत्यादि, की इस पर बड़ी तीव्रता से क्रिया होती है।
ताँबे के साथ यह क्यूप्रोटाइटेनियम, चाँदी के साथ आरजेंटोटाइटेनियम एवं ऐल्यूमिनियम के साथ कई प्रकार की मिश्रधातुएँ, जैसे (Al3Ti2) ऐ4टाइ (Al4Ti) और (Al3Ti) बनता है।
इसके सब लबण पानी में टूट जाते हैं। अम्लीय विलयन में हाइड्रोजन पेराँक्साइड, (H2O2), डालने से नारंगी रंग उत्पन्न होता है। अवकारक पदार्थ, जैसे जिंक अथवा टिन, की उपस्थिति में सल्फ्यूरिक अम्ल में टाइटेनियम के लवण नीला अथवा बैंगनी रंग देते हैं। ऐलिज़रिन सल्फोनिक अम्ल टाइटेनियम के लवणों के साथ बैंगनी रंग देते हैं।
टाइटोनियम 2, 3 तथा 4 संयोजकतावाले लवण बनाता है। जैसे (Ti F3), (Ti F4), (Ti Cl2), (Ti Cl3), (Ti Cl4), (Ti Br2), (Ti Br4), (Ti I2), (Ti I3), (Ti I4), (Ti2 S3), (Ti2 SO4), Ti2(SO4)3 तथा (Ti (SO4)2, (TiO2) से तरह तरह के टाइटेनेट, जैसे (K2 Ti3 O7), (Zn3 Ti4 O7), (Mn2 TiO4), (CoTiO3) इत्यादि बनते हैं।
टाइटेनियम बहुत से संकीर्ण यौगिक भी बनाता है और इस गुण में जिरकोनियम, हाफ्नियम तथा थोरियम से बहुत मिलता है। इसके द्विलवण भी अधिक संख्या में मिलते हैं। इसके मुख्य संकीर्ण यौगिक ऐमाइन तथा ऑक्सीजन युक्त पदार्थ, चीलेट, ऑक्सैलेट, कैटीकोल तथा हैलोजेन इत्यादि हैं।
उपयोग
संपादित करेंइसकी मिश्रधातुएँ बड़े महत्व की हैं और लोहस और अलोहस धातुओं के शोधन में काम आती हैं। इसके यौगिक कागज, कपड़ा, चमड़ा, ऊन इत्यादि रँगने तथा चीनी मिट्टी के बरतनों पर लुक करने के काम आते हैं।[2]
-
आयोडाइड प्रक्रिया से बनी टाइटानियम की क्रिस्टल छड़ी
-
टाइटानियम
-
टाइटानियम ओक्साइड - TiO2
इन्हें भी देखें
संपादित करेंसन्दर्भ
संपादित करें- ↑ "संग्रहीत प्रति". मूल से 26 अगस्त 2018 को पुरालेखित. अभिगमन तिथि 26 अगस्त 2018.
- ↑ Donachie, Matthew J., Jr. (1988). TITANIUM: A Technical Guide. Metals Park, OH: ASM International. p. 11. ISBN 0-87170-309-2.